Eosinophile Endomyokarditis (Löffler) ist selten, aber potenziell reversibel. Da in ca. 20 % keine periphere Eosinophilie besteht, darf die Diagnostik nicht allein auf das Blutbild gestützt werden. Bei arrhythmogenen Ereignissen, reduzierter LVEF oder Schock ist die Endomyokardbiopsie (EMB) richtungsweisend.
Erstpräsentation: 49-jährige Polizistin, sportlich, Vorerkrankung: Faktor-V-Leiden (ED 1998). Progrediente Belastungsintoleranz bis Dyspnoe bei minimalster Belastung. Aufnahme im Heimkrankenhaus: Vorhofflimmern (RSB), wiederholte VT (sup. Achse, RSB, pleomorph, hämodynamisch relevant), Troponin 600 ng/L. TTE: LVEF 20%, leicht dilatierter LV, funktionelle MI/TI. Notfall-Koronarangiographie ohne relevante Stenosen.
Verlauf bis Verlegung: Herz-MRT: LVEF 22%, LV-EDV 181 ml, RVEF 17%; midwall-LGE septal, nicht-ischämische Fibrose an RV-Insertionsstellen (fast transmural). LV-Thrombus. Kein typisches Myokarditis-Muster, kein Hinweis auf ARVC. DD: genetische Kardiomyopathie. Low-Output-Syndrom, rezidivierende polymorphe VTs/nsVTs, Intensivpflichtigkeit. Frühverlegung in unser Herzinsuffizienzzentrum (ZHI) zur Rekompensation, Ätiologieabklärung und Evaluation tMCS/LVAD/HTx.
Intensivstation (ZHI): Mehrere Episoden polymorpher VT, teils anhaltend, mit Hypotonie. Akut Terminierung auf Ajmalin; anschließend Amiodaron-Aufdosierung mit täglichem QTc-Monitoring (max. 480 ms). Bei persistierender Instabilität zeitweise ECLS-Indikationsprüfung; nach Rhythmusstabilisierung nicht erforderlich.
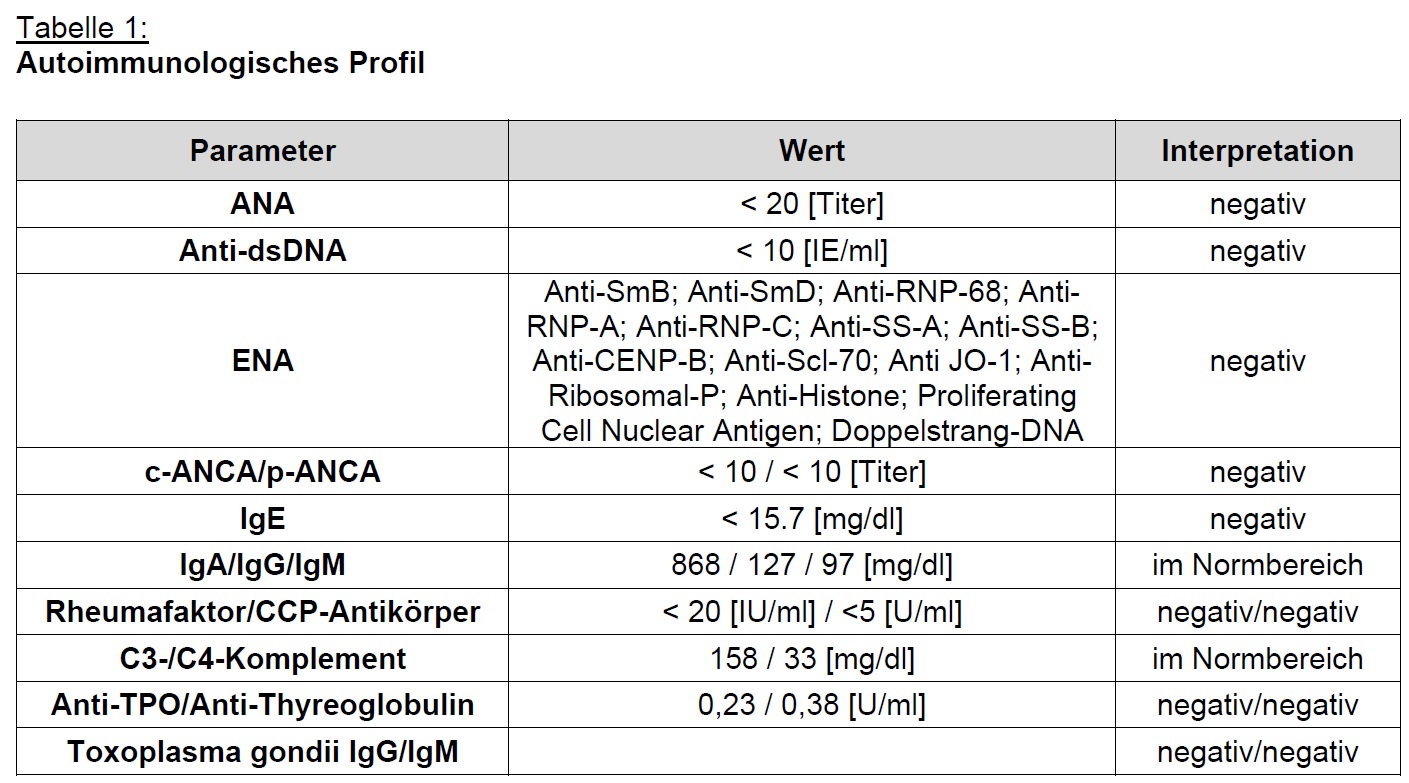
Schlüsselbefund (EMB 07/2025): Histologie: ausgeprägte eosinophile Endomyokarditis. PCR kardiotroper Erreger negativ. Kein Hinweis auf Amyloidose, Riesenzellmyokarditis oder DCM. Keine periphere Eosinophilie (Eos 170/µl zum Biopsiezeitpunkt). Autoimmunologie unauffällig (EGPA ausgeschlossen). Parasitäre Genese anamnestisch sehr unwahrscheinlich. Medikamentenreaktion möglich, konkreter Trigger nicht identifizierbar.
Therapie: Hochdosis-Steroidstoß (Methylprednisolon gesamt 3 g), dann Prednisolon-Taper. Tacrolimus (Zielspiegel 5 ng/ml) + Mycophenolat (initial 250 mg 1-0-1, später Steigerung). Schrittweise Etablierung leitliniengerechter Herzinsuffizienztherapie (GDMT) nach Inotropika-Ausschleichen. S-ICD wegen arrhythmogener Gefährdung. Vollständige Antikoagulation bei LV-Thrombus und VHF. Paralleles HTx-Work-up.
Nachkontrollen:
Tag 30 (15.08.2025): LVEF 35% (3D-TTE), NYHA II.
28.08.2025 ambulant: LVEF 45%, SR mit RSB (QRS 140 ms), NYHA I, keine ICD-Therapien. Tacrolimus beendet, MMF 1 g 1-0-1, Prednisolon 10 mg, GDMT-Auftitration.
Kontroll-EMB 10/2025: keine Eosinophilen, histologisch lymphozytäre Restmyokarditis; TTE: LVEF 43%.
Diskussion: Der Fall illustriert Vollbild einer Löffler-Endomyokarditis ohne Eosinophilie mit Dyspnoe als Erstsymptom und späterer elektrischer Instabilität bis zum Schock. Weder Blutbild noch MRT stellten die Diagnose. Die EMB war der Wendepunkt und ermöglichte sofortige Immunsuppression. Unter Steroidstoß, Tacrolimus/MMF und GDMT kam es zu einer klaren myokardialen Erholung. Der Wechsel von eosinophiler zu lymphozytärer Restinflammation in Kontroll-EMB passt zu abklingender Aktivität unter Therapie. Der S-ICD bietet Schutz in der vulnerablen Phase ohne transvenöse Elektroden.
