Hintergrund
Die Transkatheter-Aortenklappenimplantation (TAVI) führt zu einer multifaktoriellen Aktivierung hämostatischer Mechanismen, gekennzeichnet durch Hyperkoagulabilität, Hyperinflammation und gestörte Thrombozytenfunktion. Die zugrunde liegenden Mechanismen und deren Zusammenhang mit der Entstehung von Klappenthrombosen sind bislang unzureichend charakterisiert.
Methoden
In einer prospektiven, monozentrischen Studie wurden zwischen September 2022 und Juli 2024 Patienten mit TAVI eingeschlossen. Blutproben wurden am Interventionstag (T0; vor Klappenimplantation) sowie bei Entlassung (T1; Median 3,5 Tage, IQR 2–4 Tage) entnommen. Zu beiden Zeitpunkten erfolgten Analysen löslicher Biomarker mittels Standardlabor sowie zellulärer Parameter mittels Durchflusszytometrie (FACS). Eine Beurteilung auf hypodense Klappenauflagerungen (HALT) erfolgte nach 6 Monaten mittels kontrastverstärkter Computertomographie (CTA).
Ergebnisse
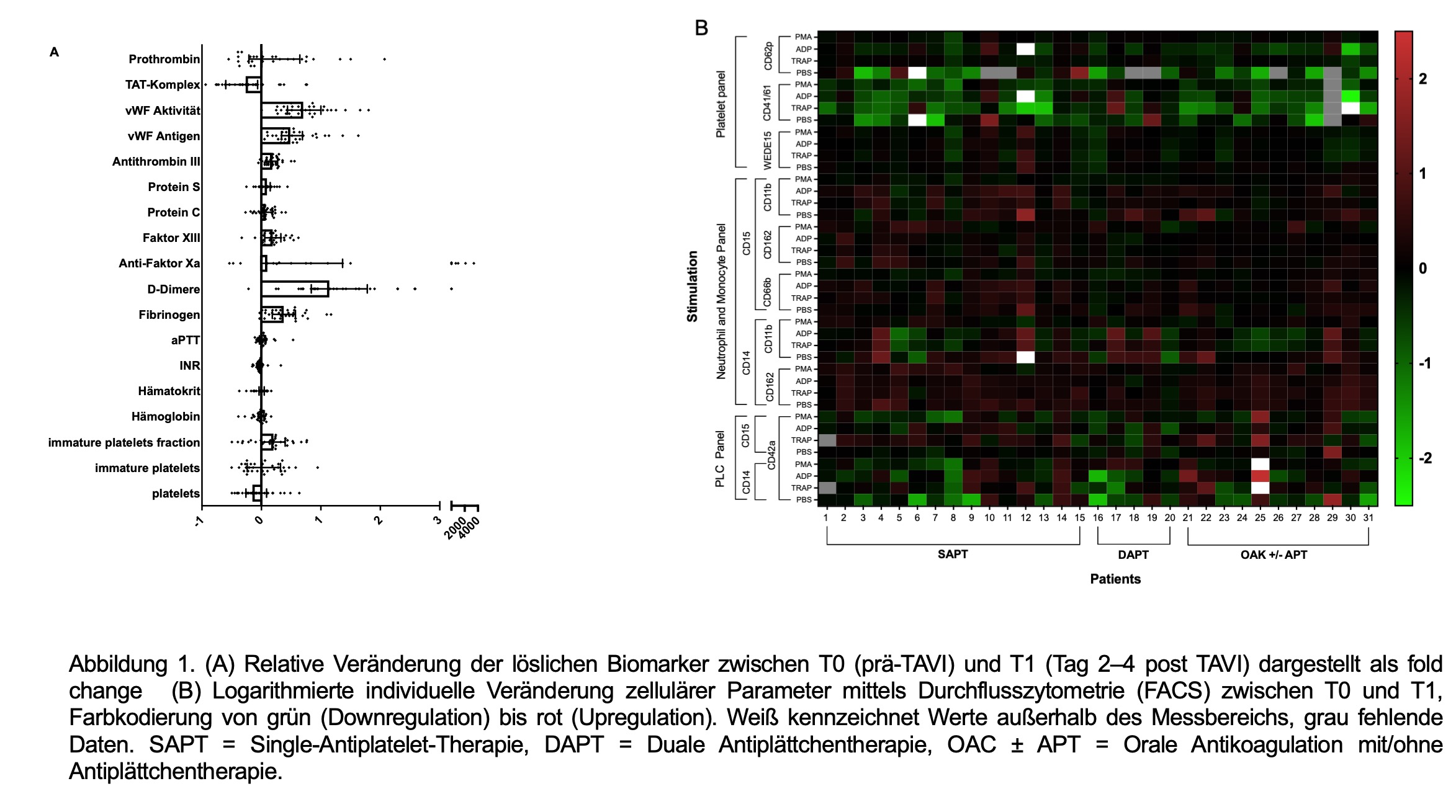
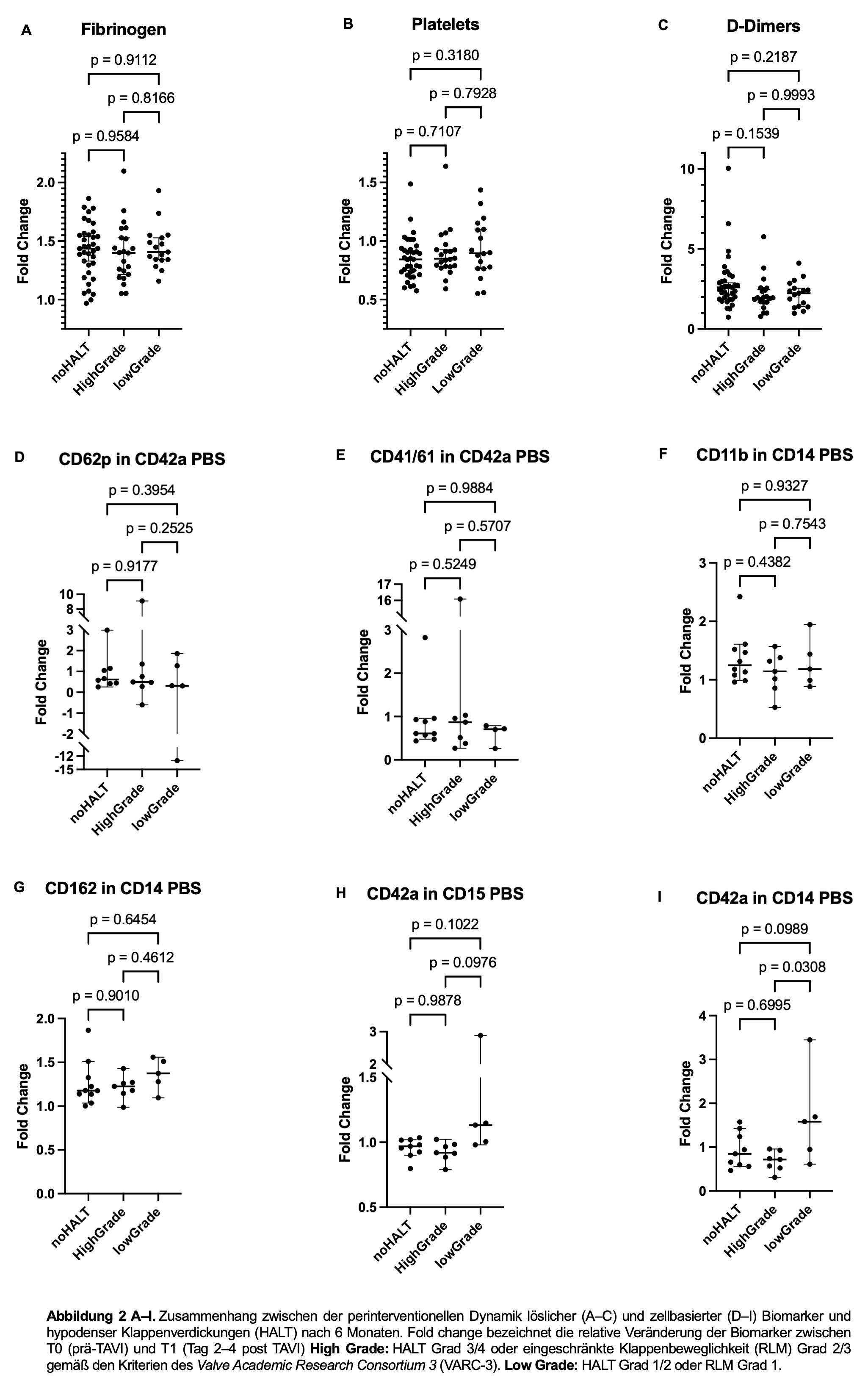
Lösliche Biomarker wurden bei 102 konsekutiven TAVI-Patienten zu T0 und T1 bestimmt, FACS-Analysen erfolgten in einer Subkohorte von 32 konsekutiven Patienten. Zwischen T0 und T1 zeigte sich ein Anstieg selektiver hämostatischer Marker als Hinweis auf periprozedurale Hyperkoagulabilität. Am ausgeprägtsten für D-Dimere (MedianΔ. 0.67mg/l [IQRΔ 0.44;1.07];p =0.001), von Willebrand-Faktor-Aktivität (MedianΔ 87% [61;116]; p < 0.0001) und Fibrinogen (MedianΔ 125 mg/dl [81;171]; p < 0.0001). (Abbildung 1 A). Ebenso zeigte sich eine Abnahme der Thrombozytenzahl (MedianΔ –27 × 10³/µl [–54.5; -5.5]; p < 0.0001), sowie der Thrombozytenfunktion, erkennbar an der reduzierten GPIIb/IIIa Expression (ΔgeoMFI –275 a.u. [–395; –93]; p < 0.0001; Abbildung 1 B). Eine inflammatorische Aktivierung mit verstärkter Thrombozyten-Leukozyten-Interaktion zeigte sich durch erhöhte Expression von CD11b auf neutrophilen Granulozyten (ΔgeoMFI 187,2 a.u. [56; 319];p=0,0068) sowie eine Zunahme von Thrombozyten-Neutrophilen-Aggregaten (CD42a⁺CD15⁺; ΔgeoMFI 377,0 a.u. [132; 569]; p = 0.036, Abbildung 1 B). Es zeigte sich keine signifikante Assoziation zwischen den periprozeduralen Veränderungen löslicher oder zellbasierter hämostatischer und inflammatorischer Marker und dem Auftreten von HALT nach 6 Monaten (Abbildung 2 A-I).
Schlussfolgerung
TAVI induziert eine multifaktorielle Aktivierung der Hämostase, charakterisiert durch Hyperkoagulabilität, Hyperinflammation und eingeschränkter Thrombozytenfunktion. Zellbasierte Analysen geben wichtige mechanistische Einblicke in diesen Prozess der Immunthrombose. Trotz ausgeprägter periprozeduraler Dynamiken von Koagulations- und Entzündungsparametern bestand keine Assoziation dieser Veränderungen mit der Entstehung von thrombotischen Auflagerungen an der Prothese nach 6 Monaten.