Klinische Charakterisierung der Arrhythmie-induzierten Kardiomyopathie: Ergebnisse einer multizentrischen prospektiven Beobachtungsstudie
Dr. Thomas Körtl, PD. Dr. Chrisitan Schach, Prof. Samuel Sossalla
Hintergrund
Rhythmusstörungen wie Vorhofflimmern (VHF) können eine arrhythmieinduzierte Kardiomyopathie (AIC), eine Unterform der dilatativen Kardiomyopathie, induzieren . Über die Inzidenz sowie über den zeitlichen Verlauf der Erholung der systolischen Funktion des linken (LV) und rechten (RV) Ventrikels ist trotz der klinisch häufigen Koexistenz von VHF und Herzinsuffizienz wenig bekannt . Bis zu einem Drittel der Patient:innen mit neu diagnostiziertem VHF haben eine Herzinsuffizienz, und bei bis zu der Hälfte der Patient:innen mit Herzinsuffizienz liegt gleichzeitig VHF vor . Das Problem bei der Diagnosestellung einer AIC besteht darin, dass diese erst im Nachhinein gestellt werden kann, wenn sich die LV-Funktion im Anschluss an eine rhythmuserhaltende Therapie erholt hat, was eine Diagnosestellung zu einem frühen Zeitpunkt erschwert .
Ziel
Ziel unserer Studie war es daher, die LV- sowie RV-Funktion bei Patient:innen mit Tachyarrhythmie und Herzinsuffizienz zu untersuchen. Der primäre Endpunkt bestand aus der Erkrankungshäufigkeit der AIC sowie der Zeit bis zur Erholung der LV-Funktion. Zudem sollten mögliche Prädiktoren zur frühen Diagnosestellung der AIC herauszuarbeitet werden.
Methoden
68 Patient:innen mit anderweitig nicht erklärbarer linksventrikulärer systolischer Dysfunktion (LVSD) (linksventrikuläre Ejektionsfraktion (LVEF) <50%) und Tachyarrhythmie (VHF/Vorhofflattern + Herzfrequenz >100/min) wurden in drei verschiedenen Zentren eingeschlossen. Andere Ursachen für eine Herzinusffizienz wurden mittels Echokardiographie, Koronarangiographie und Kardio-MRT ausgeschlossen. Nach erfolgreicher Rhythmisierung erfolgte ein Follow-up nach zwei, vier und sechs Monaten. 18 Patient:innen wurden gemäß Studienprotokoll ausgeschlossen, meist wegen rezidivierender Herzrhythmusstörungen. Die Diagnose einer AIC wurde nach sechs Monaten ex juvantibus gestellt, wenn die LVEF entweder um ≥15% oder um ≥10% mit einem insgesamten Anstieg >50% erholte. Wurden diese Kriterien nicht erfüllt, wurden die Patient:innen als non-AIC klassifiziert.
Ergebnisse
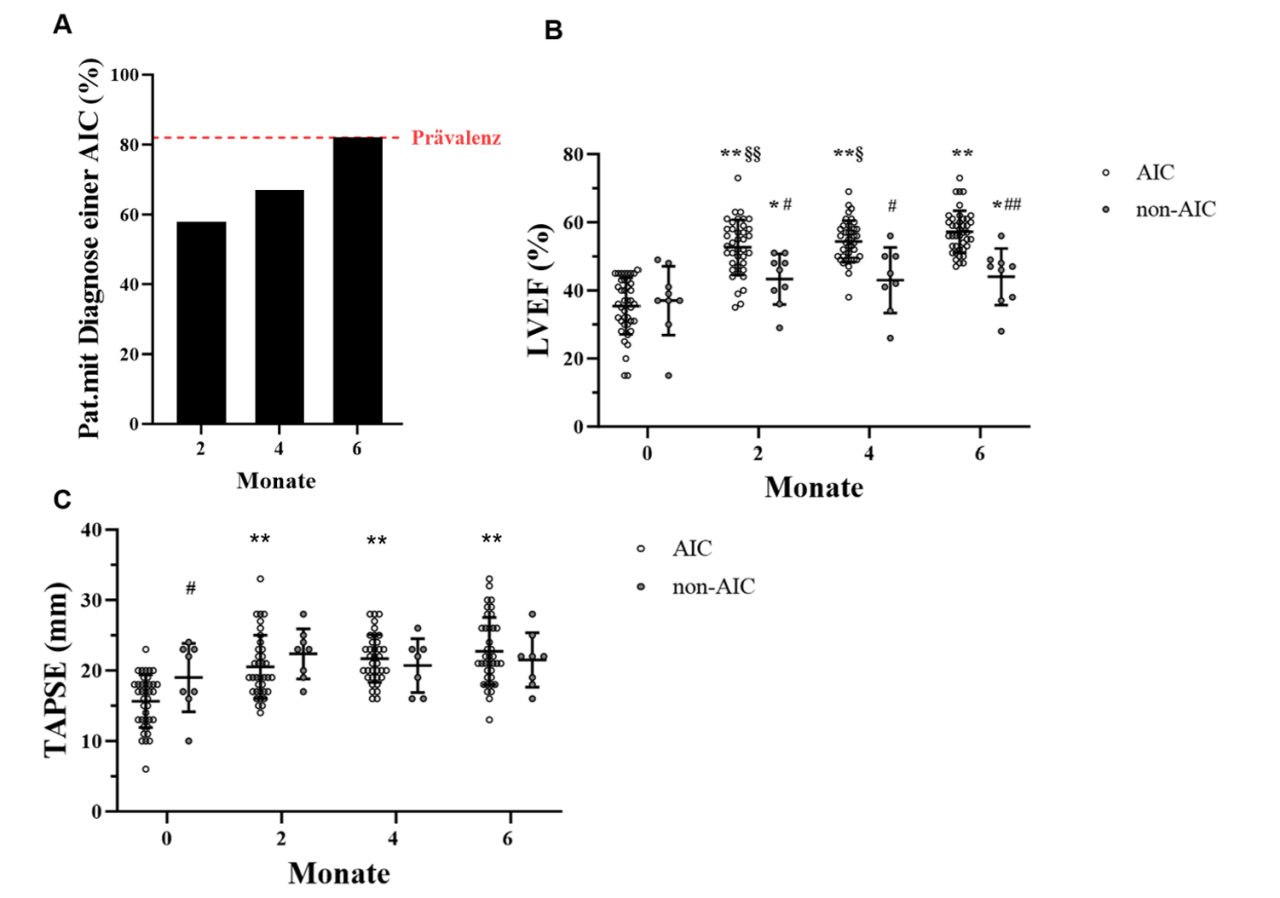
Von den 50 Patient:innen, die in die Studie aufgenommen wurden, wurde bei 41 von 50 eine AIC diagnostiziert, was einer Erkrankungshäufigkeit von 82 % entspricht. Innerhalb der ersten zwei Monate nach Rhythmuskontrolle zeigte sich bereits eine deutliche Erholung der LV-Funktion. Bei Patient:innen mit AIC stieg die LVEF von 35,4±8,2% auf 52,7±8,0% gegenüber von 37,0±9,5% auf 43,3±7,0% bei Patient:innen mit non-AIC. Ab Monat 2 bis zum Ende des Follow-ups stieg die LVEF in der AIC-Gruppe weiter auf 57,2±6,1 %, nicht jedoch in der non-AIC-Gruppe (44,0±7,8 %). Die RV-Funktion, die durch Messung der „tricuspid annular plane systolic excursion“ (TAPSE) bestimmt wurde, war bei Patient:innen mit AIC anfangs reduziert und normalisierte sich nach der Rhythmuswiederherstellung bereits nach zwei Monaten (15,7±3,7 mm auf 20,5±4,5 mm), nach sechs Monaten fand sich keine weitere signifikante Erholung (22,8±4,8 mm). In der non-AIC-Gruppe war die TAPSE initial nicht eingeschränkt und zeigte während des Nachbeobachtungszeitraums keine relevante Änderung (Abbildung 1). Durch eine multivariable Regressionsanalyse konnte festgestellt werden, dass ein kleinerer enddiastolischer LV-Durchmesser (LVEDD) bei Studienbeginn ein möglicher Parameter für die frühzeitige Diagnose einer AIC sein könnte. Hinsichtlich der Verteilung des mittels Kardio-MRT festgestellten late-gadolinium enhacements als Marker für eine Fibrose ergab sich kein sich Unterschied zwischen den Gruppen.
Schlussfolgerung/Fazit
In dieser klinisch relevanten Kohorte mit VHF ohne anderweitig erklärbarer LVSD konnte eine hohe Erkrankungshäufigkeit einer AIC festgestellt werden, was die Bedeutung dieser Erkrankung im klinischen Alltag unterstreicht. Die Erholung der LV- und RV-Funktion bei Patient:innen mit AIC findet überwiegend in den ersten zwei Monaten nach Rhythmustherapie statt. Da die weitere Erholung der LVEF bei einigen Patient:innen verzögert ist, sollte die endgültige Diagnose der AIC nach sechs Monaten gestellt werden. Der initiale LVEDD könnte ein potenzieller Prädiktor für die Früherkennung der AIC darstellen.
Referenzen
- Gopinathannair R, Etheridge SP, Marchlinski FE, Spinale FG, Lakkireddy D, Olshansky B. Arrhythmia-Induced Cardiomyopathies: Mechanisms, Recognition, and Management. J Am Coll Cardiol 2015; 66(15):1714–28.
- Sossalla S, Vollmann D. Arrhythmia-Induced Cardiomyopathy. Dtsch Arztebl Int 2018; 115(19):335–41.
- Anter E, Jessup M, Callans DJ. Atrial fibrillation and heart failure: treatment considerations for a dual epidemic. Circulation 2009; 119(18):2516–25.
- Lubitz SA, Benjamin EJ, Ellinor PT. Atrial Fibrillation in Congestive Heart Failure. Heart Fail Clin 2010; 6(2):187–200.